無水マレイン酸とアニリンを反応させると アミド結合をもつ物質が出来るのですが 無水酢酸とアニリンの反応の場合とは違い 無水マレイン酸は環構造を持っているため、どのように反応が進むのか理解できません 「化学反応式を覚えれば」問題には対処できますが反応過程が分かる方教えて高一化学について。今、〔H+〕=酸の価数×モル濃度×電離度aなどなどの所をやってるのですが、電離度が0025や0013などの時(0010やなどじゃない時)の計算の仕方が分かりません。こんな問題です。010mo 化学 解決済 教えて!goo先日溶媒として水を用いた無水酢酸と酢酸ナトリウムによるアニリンのアセチル化を行いました。手順は以下の通りです。1アニリン42 mmolに10 M塩酸42 mmolを加えてアニリン塩酸塩を調製2無水酢酸84 mmolをアニリン塩酸塩水溶液に加え、直
窒素を含む芳香族化合物
アニリン 無水酢酸 化学反応式
アニリン 無水酢酸 化学反応式-対面式授業については,状況に応じて行うことがある。 実験を通して基本的な有機化学反応(アセチル化、エステル化、縮合反応など)についての理解を深め,それらの内容を説明できるようになる。 アニリンと無水酢酸からアセトアニリドの合成2 反応式 3 実験操作 (1) 三角フラスコ(100 mL)に濃塩酸 mL (0024 mol)と水50 mLを入れ、攪拌させながら、 これにアニリン210 g (0023 mol)を少しずつ加えて溶解させる。 (2) 次に無水酢酸280 g (0027mol)を加えて攪拌し、溶解したらこれをすぐに、酢酸ナトリウ
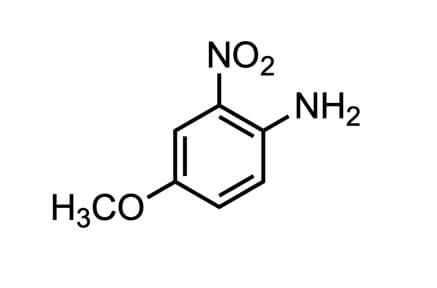


4 メトキシ 2 ニトロアニリン
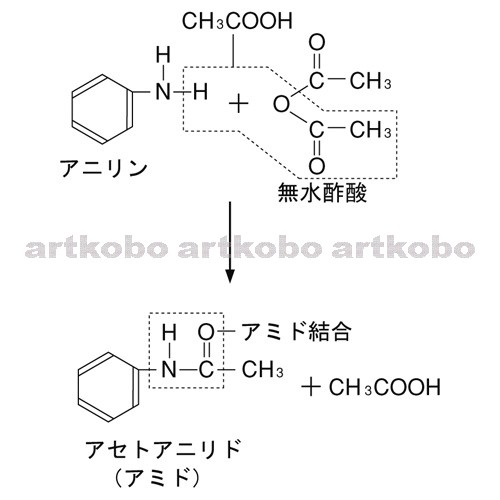
水に難溶なアニリンに塩酸を加えると、アニリン塩酸塩として水に溶ける(式1)。 酢酸ナトリウムを加えると平衡反応で、アニリンと酢酸が発生する(式2)。 発生したアニリンは、水溶液中の無水酢酸とすぐに反応してアセトアニリドになる(式3)。 5化学 無水酢酸について 無水酢酸を使うと1)サリチル酸、2)エチルアルコールから何ができるんですか?名称と反応式も書いていただけるとありがたいです。よろしくお願いします。 質問No弱塩基遊離反応について詳しくは弱酸・弱塩基遊離反応原理や公式、反応式の作り方などを確認しよう! アニリンの反応②(アセチル化) アニリンを無水酢酸(ch 3 co) 2 oと反応させると アセトアニリド が生成する。
ニトロ化号物がなぜ爆発性を示すのか?どのような化学反応が起きているのか? 無水酢酸と発煙もしくは濃硝酸を塩氷浴中で混合させて調整します。 pニトロアセトアニリドを硫酸を使って加水分解させてpニトロアニリンを合成する反応式ってどう弱塩基遊離反応について詳しくは弱酸・弱塩基遊離反応原理や公式、反応式の作り方などを確認しよう! アニリンの反応②(アセチル化) アニリンを無水酢酸(ch 3 co) 2 oと反応させると アセトアニリド が生成する。アニリンのアセチル化の実験を通じて、試薬の調合、吸引沪過、再結晶など、有機化合物の合 成に必要な基本操作を習得する。 2 反応式 ch3c o o cch3 o h n cch3 o ho cch3 o アニリン 無水酢酸 アセトアニリド 酢酸 c c c c c c n c o o c o h h h h h h c h h c h h h h c c c c c
先日溶媒として水を用いた無水酢酸と酢酸ナトリウムによるアニリンのアセチル化を行いました。手順は以下の通りです。1アニリン42 mmolに10 M塩酸42 mmolを加えてアニリン塩酸塩を調製2無水酢酸84 mmolをアニリン塩酸塩水溶液に加え、直アニリン を水に加える 。当然 ,アニリン は水に溶けない 。これに 濃塩酸 を加えると , アニリン は塩酸塩 となって 水に溶ける 。 C6H5-NH 2 + HCl → C6H5NH 3 +Cl - これに 無水酢酸 を加える 。水に難溶なアニリンに塩酸を加えると、アニリン塩酸塩として水に溶ける(式1)。 酢酸ナトリウムを加えると平衡反応で、アニリンと酢酸が発生する(式2)。 発生したアニリンは、水溶液中の無水酢酸とすぐに反応してアセトアニリドになる(式3)。 5


環化 問6



Dr Stone 漫画アニメ 化学 サルファ剤 すべての反応式 さ助ブログ
アニリンが無水酢酸と反応したときの変化を化学反応式で示すと, C 6 H 5 NH 2 +(CH 3 CO) 2 O→C 6 H 5 NHCOCH 3 +CH 3 COOH化学反応式; 解熱鎮痛剤のアスピリンを覚えていますね。サリチル酸に無水酢酸を作用させると,ヒドロキシル基の部分が反応してアセチルサリチル酸になりました。 アニリンに酢酸を加えて熱し縮合させるか,無水酢酸でアセチル化すると,アミド酢酸(許容慣用名) エタン酸(系統名) 識別情報 CAS登録番号 E番号 E260 (防腐剤) KEGG C SMILES CC(=O)O 特性 化学式 C 2 H 4 O 2 モル質量 6005 示性式 CH 3 COOH 外観 無色の液体 密度 1049(液体) 相対蒸気密度 21 融点 167 °C , 290 K, 62 °F 沸点 118 °C , 391 K, 244 °F 酸解離定数 p K a 476 屈折率 (n D) 1


医療工学科の化学講義 26 窒素を含む有機化合物 Life Chemistry


収率の計算はこういうふうにやるのです Life Chemistry
先日溶媒として水を用いた無水酢酸と酢酸ナトリウムによるアニリンのアセチル化を行いました。手順は以下の通りです。1アニリン42 mmolに10 M塩酸42 mmolを加えてアニリン塩酸塩を調製2無水酢酸84 mmolをアニリン塩酸塩水溶液に加え、直水に難溶なアニリンに塩酸を加えると、アニリン塩酸塩として水に溶ける(式1)。 酢酸ナトリウムを加えると平衡反応で、アニリンと酢酸が発生する(式2)。 発生したアニリンは、水溶液中の無水酢酸とすぐに反応してアセトアニリドになる(式3)。 5



アセチル化について教えてください Okwave


芳香族アミンを網羅的に解説 受験メモ
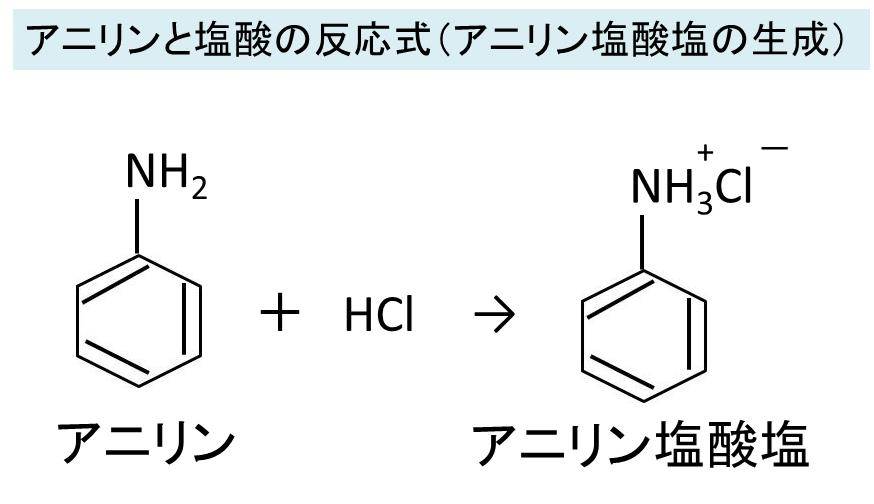


アニリンと塩酸の反応式 アニリン塩酸塩生成 やアニリン塩酸塩と水酸化ナトリウムの反応式



高校化学 アニリンと無水酢酸の反応 練習編 映像授業のtry It トライイット



有機反応を俯瞰する ー縮合反応 Chem Station ケムステ



Wo05 0905号 微生物及び微生物由来酵素によるアニリン誘導体のアセチル化 Astamuse



有機反応を俯瞰する ー縮合反応 Chem Station ケムステ
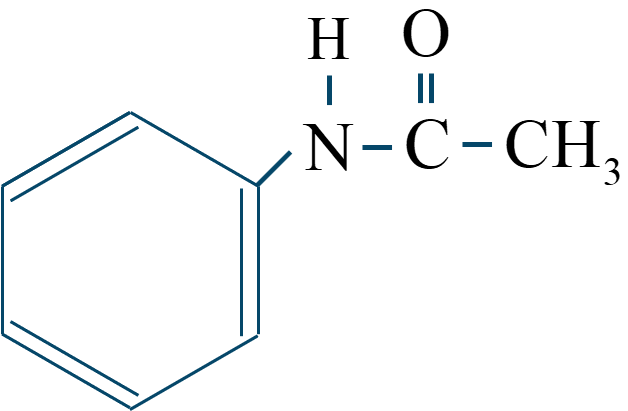


有機化学のまとめと効率的暗記 芳香族アミン ページ 3 耳たこ高校化学暗記帳
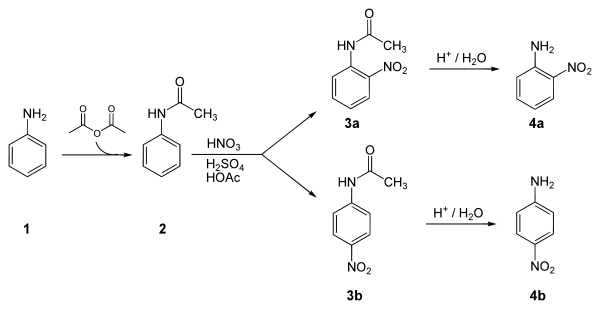


4 ニトロアニリン Wikipedia


3 6 5 アミドの反応 Yaku Tik 薬学まとめました
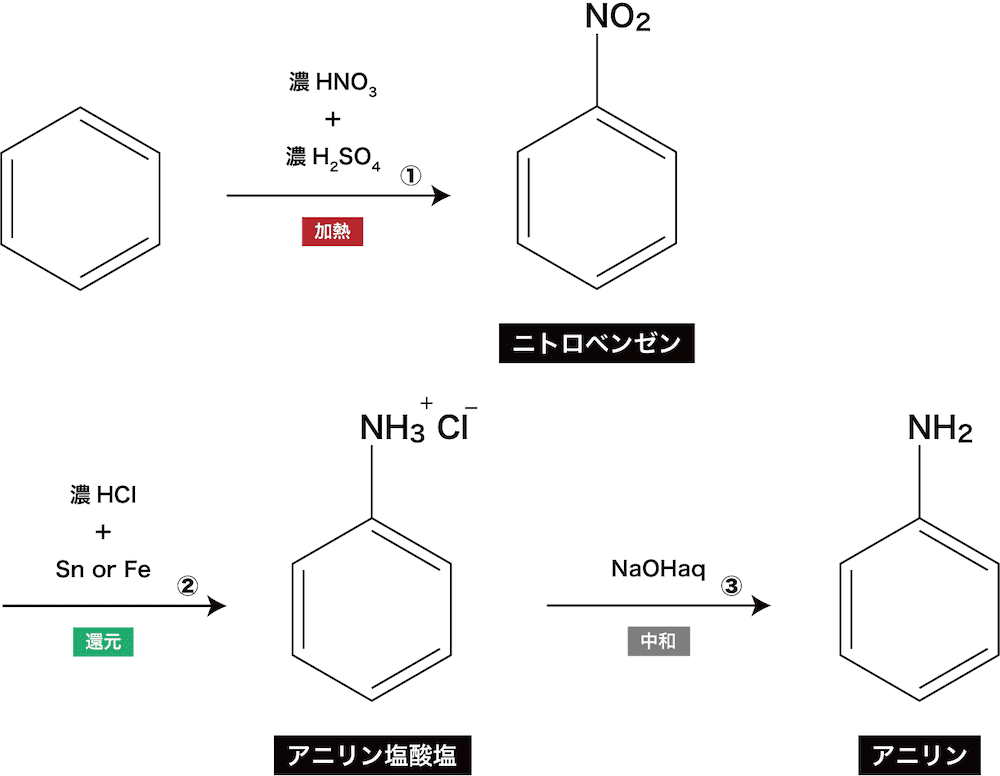


芳香族アミン アニリン の構造 製法 性質 反応 化学のグルメ
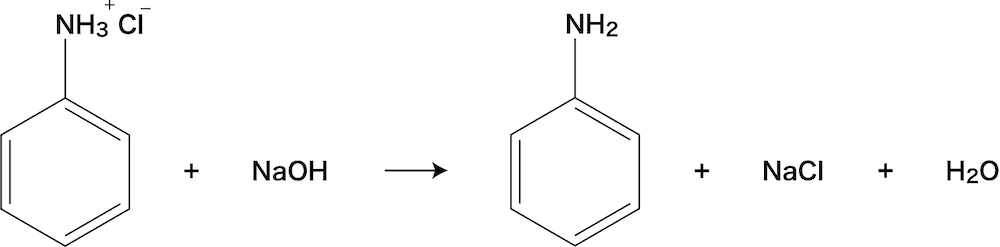


芳香族アミン アニリン の構造 製法 性質 反応 化学のグルメ
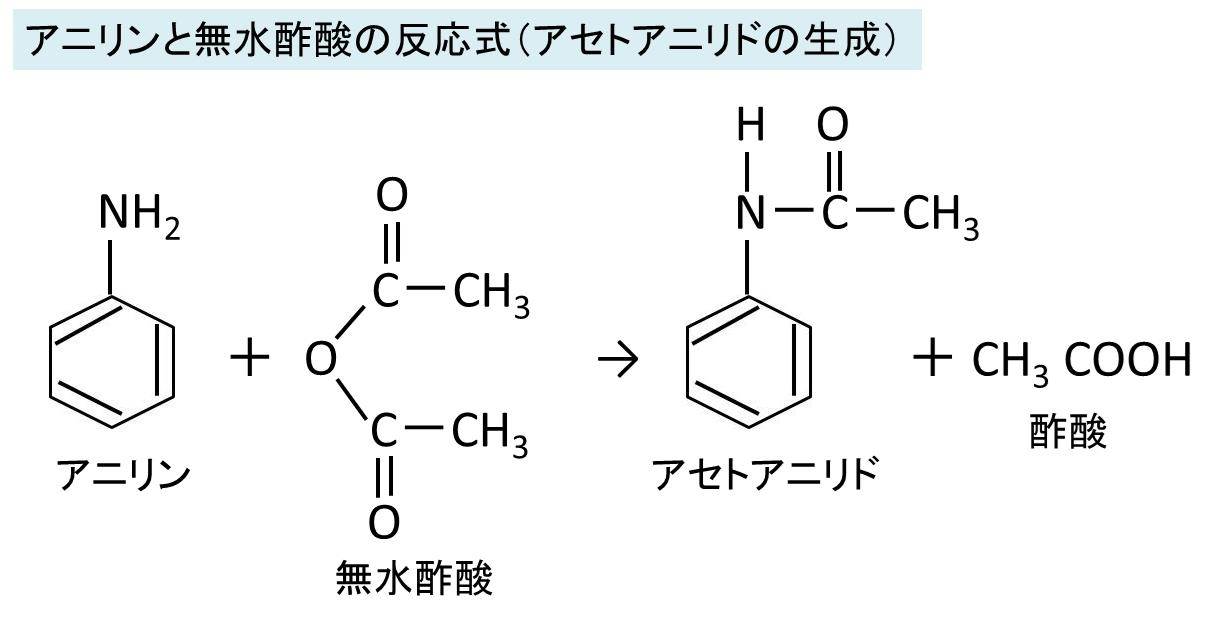


アニリンと無水酢酸の反応式 アセトアニリド生成 酢酸を使用しない理由は


窒素を含む芳香族化合物



アゾカップリングは染料を合成する工業的化学反応 とらおの有機化学



有機反応を俯瞰する ー縮合反応 Chem Station ケムステ



アニリンのニトロ化 Okwave
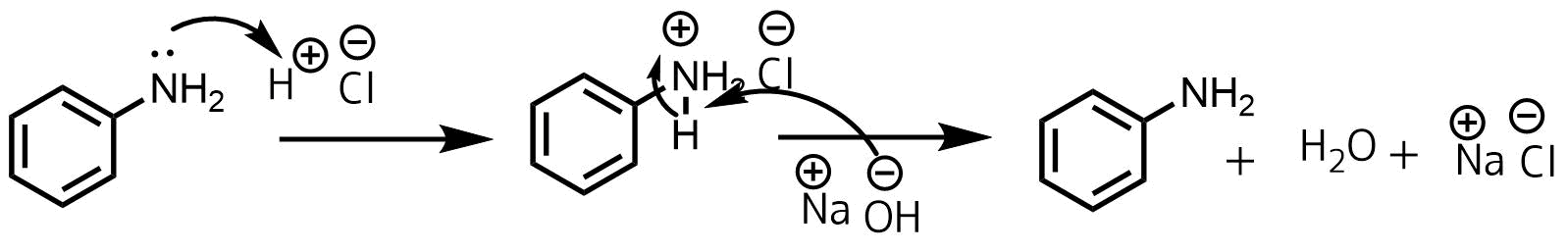


アニリン塩酸塩 Anilinium Chloride Japaneseclass Jp


Web教材イラスト図版工房 R Ch 芳香族化合物 56
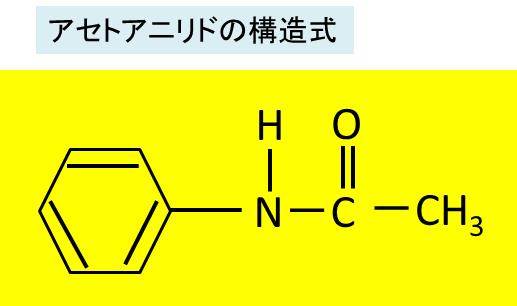


アセトアニリドの化学式 分子式 構造式 分子量は



4 メトキシ 2 ニトロアニリン



アニリンのニトロ化の生成過程 反応中間体の共鳴式 アニリンをニトロ 化学 教えて Goo



有機反応を俯瞰する ー縮合反応 Chem Station ケムステ


第137章 医薬品



無水酢酸 健康用語web事典



4 ニトロアニリン Wikipedia



アニリン Chemihack おうちで学べる化学
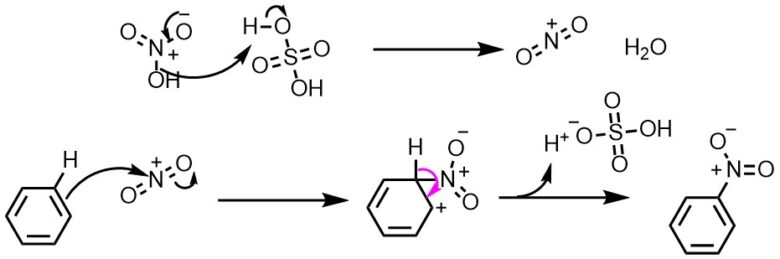


ニトロ化反応の条件とやり方 ネットdeカガク



高等学校化学i 芳香族化合物 アニリンとアゾ化合物 Wikibooks


学位論文要旨詳細


放課後化学講義室 今日の分子
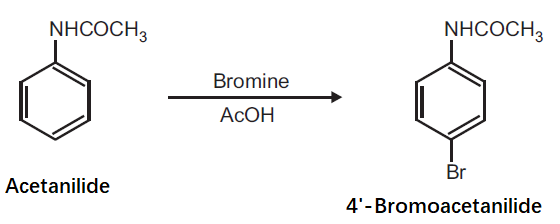


4 ブロモアセトアニリド 103 8


無料ダウンロード 無水酢酸 構造式 人気のある画像を投稿する



ニンヒドリン反応の利用法と反応機構



有機反応を俯瞰する ー縮合反応 Chem Station ケムステ



高校化学 アニリンと無水酢酸の反応 練習編 映像授業のtry It トライイット



無料ダウンロード 無水酢酸 構造式 人気のある画像を投稿する


学位論文要旨詳細
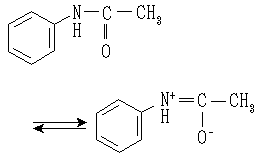


アセトアニリドとは コトバンク
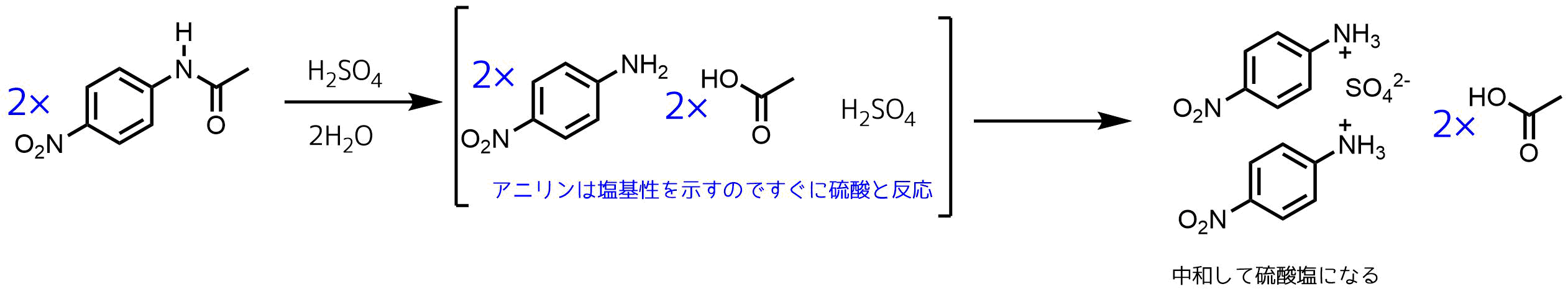


ニトロ化反応の条件とやり方 ネットdeカガク


神大工応化 有機化学iii


質問です 有機化学で このアセトアニリドの共鳴に関する反応機構は正しいでしょう Yahoo 知恵袋



フェノール類とアニリンの呈色反応の語呂合わせ 18h30大学入学共通テスト試行調査第2回第3問b 入試化学を語呂合わせで解く大学入試ゴロ化学


アセトアニリドをアニリンと無水酢酸から合成する実験を行いました そ Yahoo 知恵袋



アセトアニリド Wikipedia



4 ジメチルアミノピリジン Wikipedia


芳香族アミンを網羅的に解説 受験メモ



Images Of アセトアニリド Japaneseclass Jp
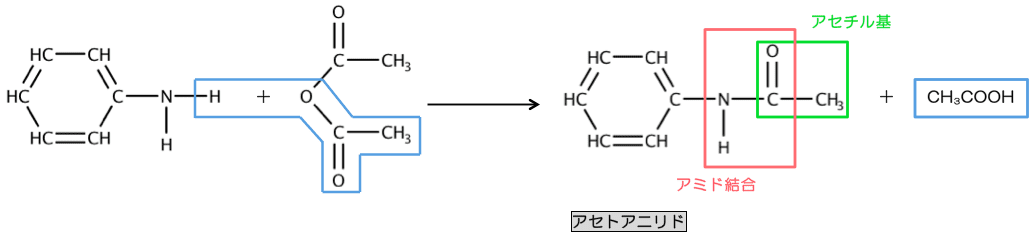


芳香族アミン 高校化学 化学基礎一問一答 化学のグルメ



アセトアニリド 分子量 4
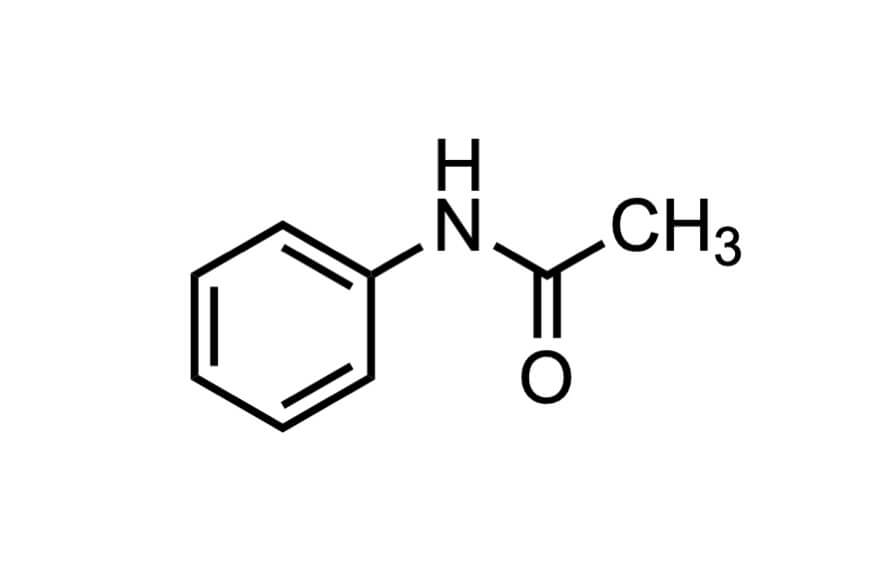


アセトアニリド


有機化学のオキテ25 医学部予備校レクサス教育センター



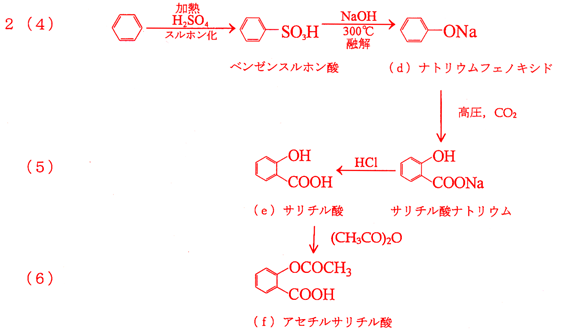
サリチル酸 とサリチル酸メチルとアセチルサリチル酸 の構造式と医学的利用 Irohabook



Dr Stone 漫画アニメ 化学 サルファ剤 すべての反応式 さ助ブログ


アニリンと無水酢酸 酢酸で反応させてアセトアニリドを生成させる Yahoo 知恵袋


環化 問6



高校化学 芳香族化合物の構造式 Flashcards Quizlet


4k有機化学 章末問題こたえ



アニリンの性質と製法 塩化ベンゼンジアゾニウムとpヒドロキシアゾベンゼン Irohabook



アセトアミノフェン Wikiwand
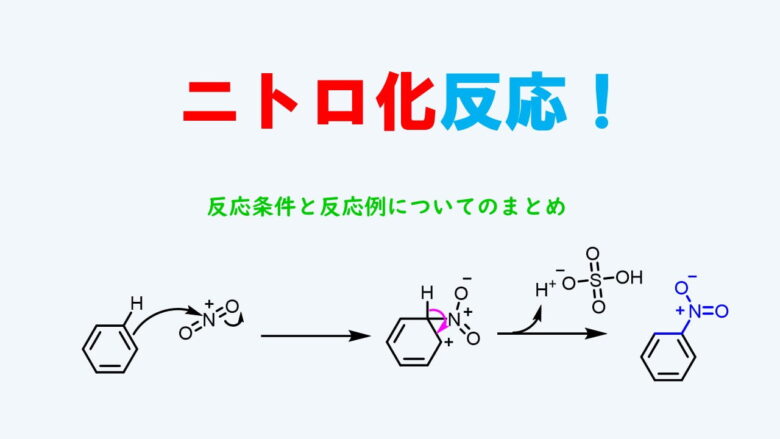


ニトロ化反応の条件とやり方 ネットdeカガク


名城大学理工学部応用化学科 永田研究室 有機化学演習 第10回疑問点など


1


アニリン 合成 アセトアニリドの反応機構を示せ という課題に対して画 Yahoo 知恵袋



Wo05 0905号 微生物及び微生物由来酵素によるアニリン誘導体のアセチル化 Astamuse


P ニトロアセトアニリドからp ニトロアニリンへの反応機構 Okwave



高校化学 アニリンと無水酢酸の反応 映像授業のtry It トライイット
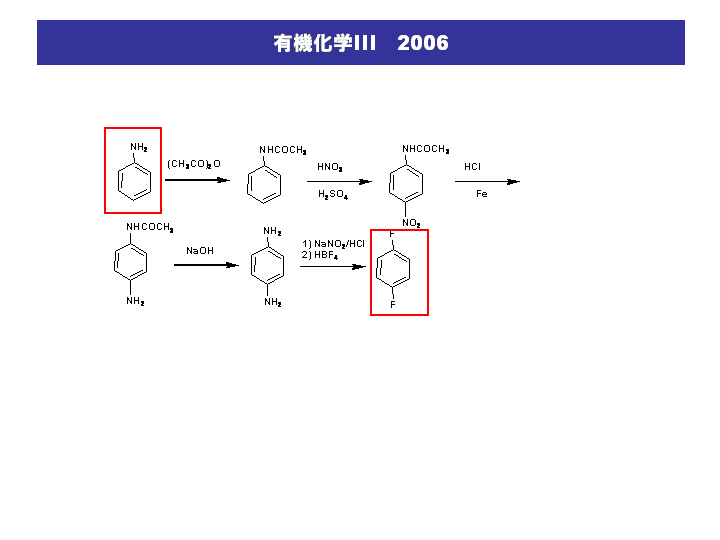


神大工応化 有機化学iii



アニリン塩酸塩はベンゼンにnh3 とcl なので Clear



エステル化など絶対に押さえておくべきカルボン酸の反応5選 化学受験テクニック塾
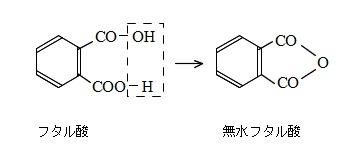


芳香族カルボン酸 安息香酸とフタル酸とサリチル酸



高校化学 アニリンと無水酢酸の反応 映像授業のtry It トライイット



アニリン塩酸塩はベンゼンにnh3 とcl なので Clear


1



Sandmeyer反応はアニリンを起点とする官能基導入法 とらおの有機化学
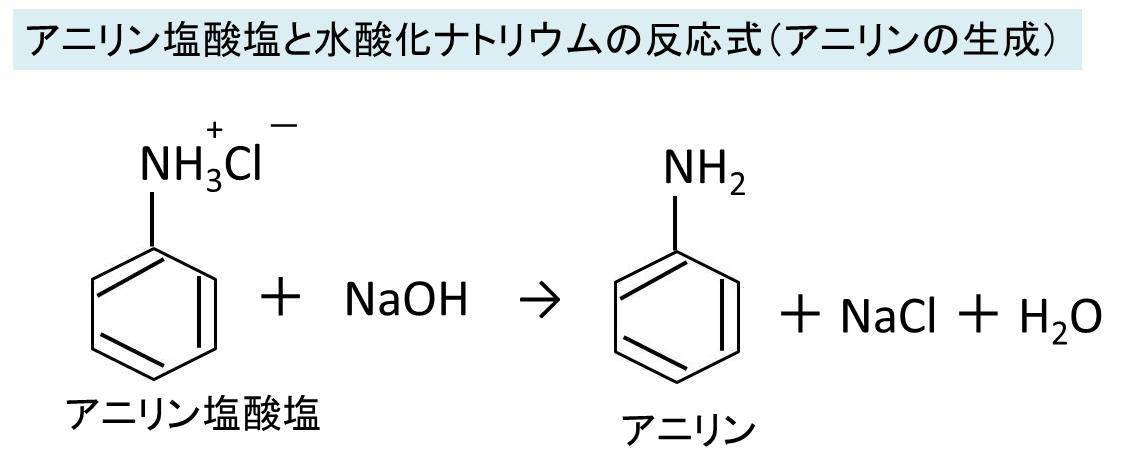


アニリンと塩酸の反応式 アニリン塩酸塩生成 やアニリン塩酸塩と水酸化ナトリウムの反応式



アニリン Chemihack おうちで学べる化学



高等学校化学i 芳香族化合物 アニリンとアゾ化合物 Wikibooks


カルボニル化合物 カルボン酸誘導体


有機反応機構 カルボン酸とその誘導体の反応



酢酸 Wikiwand


第137章 医薬品



無料ダウンロード 無水酢酸 構造式 人気のある画像を投稿する
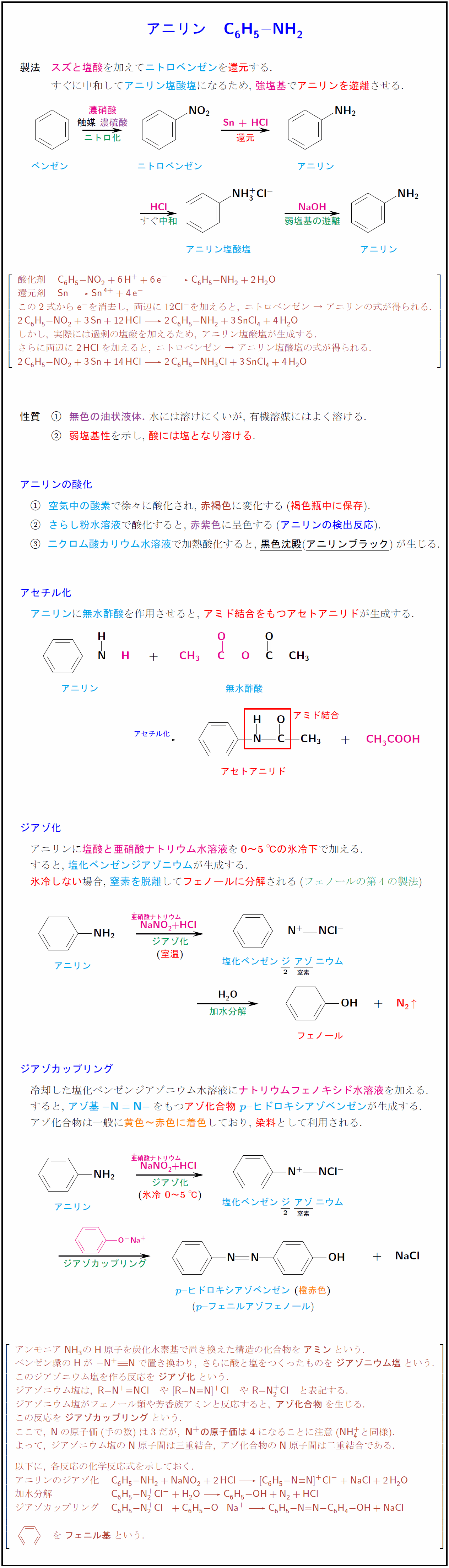


高校有機化学 アニリン C H Nh の製法 酸化 アセチル化 ジアゾ化 ジアゾカップリング 受験の月
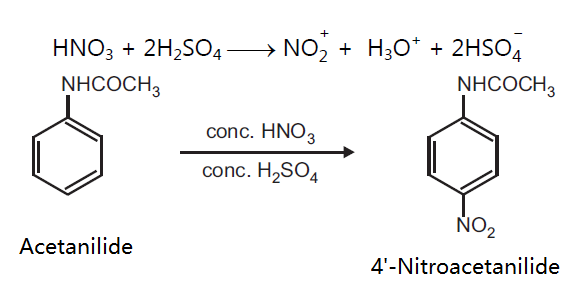


4 ニトロアセトアニリド 104 04 1



アセチル化について教えてください ある物質をアセチル化するのに無 化学 教えて Goo



Dr Stone 漫画アニメ 化学 サルファ剤 すべての反応式 さ助ブログ



0 件のコメント:
コメントを投稿